Le marché mondial des dispositifs médicaux connaît une croissance exponentielle, et avec lui, la demande de pièces plastiques de haute précision. En 2026, l'injection de pièces plastiques pour dispositifs médicaux représente un secteur stratégique où convergent excellence technique, conformité réglementaire stricte et innovation technologique. Chaque composant, du boîtier d'un appareil de diagnostic à l'implant chirurgical, doit répondre à des exigences de qualité sans compromis. Mais comment garantir cette perfection dans un environnement aussi réglementé ? Quelles sont les techniques qui transforment le secteur en 2026 ?

Table des Matières
- Les Fondamentaux de l'Injection Plastique pour le Médical
- Techniques d'Injection Avancées en 2026
- Matériaux et Biocompatibilité
- Normes et Certifications Obligatoires
- Process de Fabrication et Contrôle Qualité
- Tendances et Innovations 2026
Les Fondamentaux de l'Injection Plastique pour le Médical
Principe du Moulage par Injection
Le moulage par injection plastique est un procédé de fabrication qui consiste à injecter un polymère fondu sous haute pression dans un moule de précision. Une fois refroidi, le matériau se solidifie pour prendre la forme exacte de la cavité du moule. Ce processus, répété des milliers de fois, permet de produire des pièces identiques avec une tolérance dimensionnelle exceptionnelle.
Pour les dispositifs médicaux, ce procédé s'accompagne de contraintes spécifiques : traçabilité complète de chaque lot, validation exhaustive du process, et environnement de production contrôlé. Chaque paramètre d'injection (température, pression, vitesse, temps de refroidissement) doit être documenté et maintenu dans des plages étroites pour garantir la reproductibilité.
Spécificités du Secteur Médical
L'injection de pièces plastiques pour dispositifs médicaux se distingue radicalement de l'injection industrielle standard. Les différences fondamentales incluent :
Environnement de production : Les pièces médicales sont fabriquées en salle blanche ISO 7 ou ISO 8, où le nombre de particules en suspension est strictement contrôlé. L'air est filtré en continu, et les opérateurs portent des équipements de protection spécifiques pour éviter toute contamination.
Matériaux certifiés : Seuls les polymères biocompatibles, testés selon la norme ISO 10993, peuvent être utilisés. Ces matériaux ne doivent provoquer aucune réaction toxique, allergique ou inflammatoire au contact du corps humain.
Documentation exhaustive : Chaque étape du processus doit être tracée et archivée. Le Device History Record (DHR) accompagne chaque lot de production et permet une traçabilité totale, du granulé de polymère au dispositif fini.
📊 78% des fabricants de dispositifs médicaux ont augmenté leurs investissements dans l'injection plastique en 2026 - Croissance du marché
Différence avec l'Injection Industrielle Standard
| Critère | Injection Industrielle | Injection Médicale |
|---|---|---|
| Environnement | Atelier standard | Salle blanche ISO 7/8 |
| Traçabilité | Par lot | Pièce par pièce possible |
| Validation | Qualification initiale | Validation continue + revalidation |
| Matériaux | Polymères standards | Polymères biocompatibles certifiés |
| Documentation | Minimale | Exhaustive (DHR, DMR) |
| Coût de production | Standard | +40% à +200% |
Techniques d'Injection Avancées en 2026
L'année 2026 marque un tournant dans les technologies d'injection plastique pour le médical. Les fabricants adoptent des techniques de plus en plus sophistiquées pour répondre aux exigences de miniaturisation et de fonctionnalité.
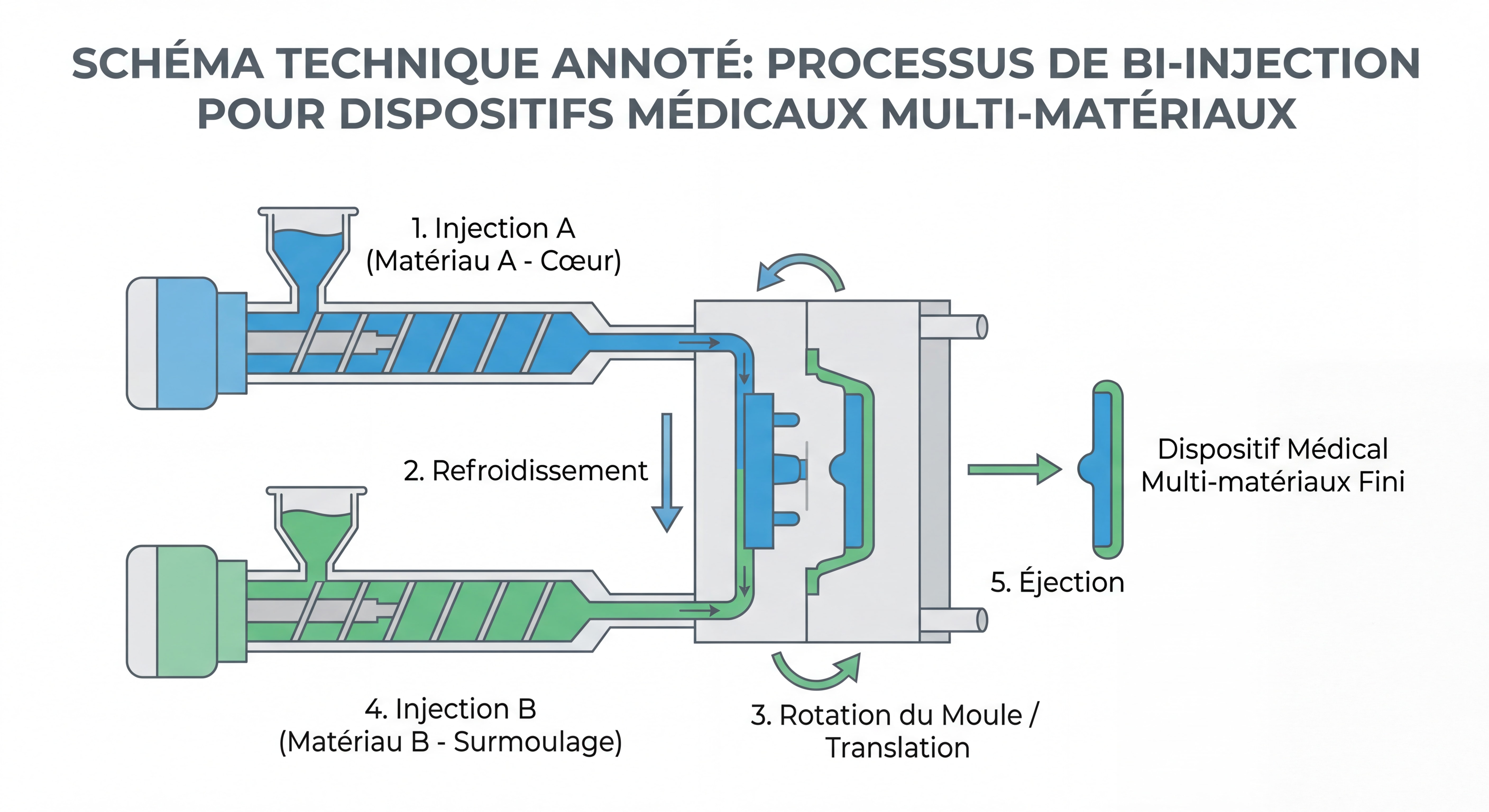
Moulage Bi-Injection
La bi-injection (ou injection bi-matière) permet de combiner deux polymères différents dans une seule pièce, en une seule opération. Cette technique révolutionne la conception des dispositifs médicaux en 2026, notamment pour :
- Poignées ergonomiques : Combinaison d'un polymère rigide pour la structure et d'un élastomère souple pour le confort de préhension
- Joints d'étanchéité intégrés : Assemblage d'un corps rigide avec un joint souple sans étape d'assemblage secondaire
- Dispositifs multi-fonctions : Intégration de zones transparentes et opaques, ou de zones conductrices et isolantes
Les avantages de la bi-injection incluent la réduction des coûts d'assemblage, l'élimination des colles et adhésifs (sources potentielles de contamination), et l'amélioration de la fiabilité du produit final.
Injection Assistée par Gaz
L'injection assistée par gaz (Gas Assisted Injection Molding - GAIM) consiste à injecter un gaz inerte (généralement de l'azote) dans le polymère fondu pendant le processus d'injection. Cette technique crée des canaux creux à l'intérieur de la pièce, permettant :
- Réduction du poids des dispositifs (jusqu'à 30%)
- Diminution des contraintes résiduelles et du gauchissement
- Amélioration de la stabilité dimensionnelle
- Réduction du temps de cycle et de la consommation de matière
En 2026, cette technique est particulièrement prisée pour les dispositifs portables et les équipements de diagnostic ambulatoires, où le poids est un critère critique.
Micro-Injection pour Dispositifs Miniaturisés
La micro-injection permet de fabriquer des pièces de quelques milligrammes avec des tolérances de l'ordre du micromètre. Cette technique est essentielle pour :
- Implants ophtalmiques : Lentilles intraoculaires, anneaux cornéens
- Composants de cathéters : Connecteurs miniatures, valves anti-retour
- Dispositifs de drug delivery : Micro-aiguilles, pompes implantables
"La micro-injection représente le futur de l'industrie médicale, permettant des interventions moins invasives et plus précises"
— Dr. Marie Dubois, Directrice R&D MedTech Europe
Les machines de micro-injection utilisées en 2026 intègrent des systèmes de contrôle ultra-précis, avec des capteurs en temps réel pour chaque paramètre d'injection, garantissant une répétabilité exceptionnelle.
Technologies Émergentes
Injection séquentielle multi-composants : Cette technique permet d'injecter successivement plusieurs matériaux dans des zones spécifiques du moule, créant des pièces avec des propriétés graduées.
Moulage par compression assisté par injection : Combinaison des avantages de l'injection et de la compression pour produire des pièces ultra-minces avec d'excellentes propriétés optiques, idéales pour les dispositifs de diagnostic.
Injection avec inserts métalliques ou électroniques : Intégration de composants métalliques (contacts électriques, renforts) ou électroniques (puces RFID, capteurs) directement pendant l'injection, réduisant les étapes d'assemblage.
Matériaux et Biocompatibilité
Le choix du matériau constitue l'une des décisions les plus critiques dans le développement d'un dispositif médical. En 2026, la palette de polymères biocompatibles s'est considérablement élargie, offrant des solutions pour chaque application.
Polymères Biocompatibles Certifiés
PEEK (Polyétheréthercétone) : Polymère haute performance présentant une résistance mécanique exceptionnelle et une biocompatibilité remarquable. Le PEEK est utilisé pour les implants orthopédiques, les instruments chirurgicaux réutilisables et les composants de dispositifs implantables. Il supporte la stérilisation répétée (autoclave, rayons gamma) sans dégradation de ses propriétés.
UHMWPE (Polyéthylène Ultra-Haute Masse Moléculaire) : Matériau de référence pour les implants articulaires (prothèses de hanche, de genou). L'UHMWPE offre une résistance à l'usure exceptionnelle et une biocompatibilité prouvée sur plusieurs décennies d'utilisation clinique.
Silicones médicaux : Les élastomères de silicone sont incontournables pour les applications nécessitant souplesse et biocompatibilité. Ils sont utilisés pour les cathéters, les valves cardiaques, les implants mammaires et de nombreux dispositifs en contact prolongé avec les tissus.
Polycarbonate (PC) médical : Transparent, résistant aux chocs, le PC médical est le matériau de choix pour les dispositifs nécessitant une visualisation (réservoirs de perfusion, connecteurs transparents, boîtiers de pompes).
Polypropylène (PP) médical : Économique et polyvalent, le PP médical est utilisé pour les seringues, les conteneurs à usage unique, et de nombreux dispositifs jetables.
Tests de Biocompatibilité (ISO 10993)
La norme ISO 10993 définit l'évaluation biologique des dispositifs médicaux. Elle comprend une série de tests obligatoires selon le type et la durée de contact du dispositif avec le corps :
| Type de Contact | Durée | Tests Requis |
|---|---|---|
| Contact limité | < 24h | Cytotoxicité, Sensibilisation |
| Contact prolongé | 24h - 30 jours | + Irritation, Toxicité systémique |
| Contact permanent | > 30 jours | + Implantation, Hemocompatibilité, Carcinogénicité |
| En 2026, les tests de biocompatibilité s'accompagnent d'analyses d'extractibles et de relargables (Extractables & Leachables), identifiant toute substance susceptible de migrer du polymère vers les tissus biologiques. | ||
Choix du Matériau selon l'Application
Dispositifs implantables : PEEK, UHMWPE, titane revêtu de polymère. Exigences : biocompatibilité à long terme, résistance à la fatigue, stabilité dimensionnelle.
Dispositifs de diagnostic in vitro : Polystyrène, polypropylène. Exigences : transparence, inertie chimique, faible coût.
Dispositifs chirurgicaux réutilisables : PEEK, polyétherimide (PEI), polysulfone (PSU). Exigences : résistance à la stérilisation répétée, stabilité dimensionnelle, résistance chimique.
Dispositifs à usage unique : Polypropylène, polyéthylène, PVC médical. Exigences : coût optimisé, processabilité, conformité réglementaire.
📊 34% d'augmentation de l'utilisation de polymères biosourcés dans les dispositifs médicaux entre 2024 et 2026 - Croissance des biopolymères
Normes et Certifications Obligatoires
L'industrie des dispositifs médicaux est l'une des plus réglementées au monde. En 2026, les exigences de conformité continuent de se renforcer, avec une attention particulière portée à la traçabilité et à la gestion des risques.
ISO 13485 : Exigences Système Qualité
L'ISO 13485 est la norme internationale définissant les exigences relatives aux systèmes de management de la qualité pour les organismes impliqués dans la conception, la production, l'installation et la maintenance de dispositifs médicaux.
Principes fondamentaux :
- Approche par les risques (gestion des risques selon ISO 14971)
- Validation des processus de production et de service
- Traçabilité complète des produits
- Gestion rigoureuse des non-conformités et des actions correctives
- Contrôle strict des fournisseurs et sous-traitants
La certification ISO 13485 est un prérequis absolu pour commercialiser des dispositifs médicaux en Europe et dans la plupart des marchés internationaux. Les audits de surveillance sont réalisés annuellement, et la recertification complète intervient tous les trois ans.
FDA 21 CFR Part 820
Le 21 CFR Part 820 est le règlement américain définissant les Quality System Regulations (QSR) pour les fabricants de dispositifs médicaux. Il couvre l'ensemble du cycle de vie du produit :
- Design Controls : Maîtrise de la conception et du développement
- Production and Process Controls : Contrôle de la production et des processus
- CAPA (Corrective and Preventive Actions) : Actions correctives et préventives
- Device History Record (DHR) : Dossier historique du dispositif
- Device Master Record (DMR) : Dossier maître du dispositif

Marquage CE Dispositifs Médicaux
Le règlement européen (UE) 2017/745 sur les dispositifs médicaux (MDR), pleinement applicable depuis 2026, impose des exigences renforcées :
Classification des dispositifs : Les dispositifs sont classés de la classe I (risque faible) à la classe III (risque élevé). La classification détermine le niveau de contrôle réglementaire.
Évaluation de la conformité : Selon la classe, l'évaluation peut nécessiter l'intervention d'un organisme notifié, qui audite le système qualité et examine la documentation technique.
Base de données EUDAMED : Depuis mai 2026, l'enregistrement dans la base de données EUDAMED est obligatoire pour tous les dispositifs commercialisés en Europe. Cette base assure la traçabilité et la surveillance post-commercialisation.
"L'application renforcée du règlement MDR généralise les équipements marqués CE et impose une traçabilité accrue des dispositifs médicaux"
— Règlement (UE) 2017/745
Traçabilité et Documentation
La traçabilité est le fil rouge de la conformité réglementaire. Chaque dispositif médical doit pouvoir être retracé depuis les matières premières jusqu'au patient final. Cette traçabilité s'appuie sur :
UDI (Unique Device Identification) : Code unique attribué à chaque dispositif, permettant son identification sans ambiguïté dans les bases de données réglementaires.
Batch Records : Enregistrements de lot documentant tous les paramètres de production, les contrôles effectués, et les déviations éventuelles.
Traçabilité des matières premières : Certificats de conformité des polymères, attestations de biocompatibilité, analyses de lots.
Process de Fabrication et Contrôle Qualité
La fabrication de pièces plastiques pour dispositifs médicaux exige un niveau de rigueur sans équivalent dans l'industrie. Chaque étape est contrôlée, validée et documentée.
Environnement Salle Blanche
Les salles blanches sont des environnements contrôlés où la concentration de particules en suspension est maintenue à des niveaux extrêmement bas. Les classes ISO 7 et ISO 8 sont les plus couramment utilisées pour l'injection plastique médicale :
- ISO 7 : Maximum 352 000 particules ≥ 0,5 µm par m³
- ISO 8 : Maximum 3 520 000 particules ≥ 0,5 µm par m³
Ces environnements nécessitent : - Systèmes de filtration HEPA (High Efficiency Particulate Air)
- Surpression positive pour éviter l'entrée de contaminants
- Contrôle de température et d'humidité
- Protocoles stricts d'habillage et de comportement du personnel
- Nettoyage et désinfection réguliers selon des procédures validées

Validation du Process
La validation du processus d'injection est une exigence réglementaire fondamentale. Elle démontre que le processus produit de manière reproductible des pièces conformes aux spécifications.
IQ (Installation Qualification) : Vérification que l'équipement est installé conformément aux spécifications du fabricant et aux exigences du site.
OQ (Operational Qualification) : Démonstration que l'équipement fonctionne selon les paramètres définis, dans toutes les conditions d'utilisation prévues.
PQ (Performance Qualification) : Validation que le processus complet produit des pièces conformes de manière répétée. Généralement réalisée sur 3 lots consécutifs (approche 3x3x3).
La revalidation est nécessaire en cas de changement significatif (nouveau moule, nouveau matériau, modification de paramètres, déménagement d'équipement).
Contrôles en Cours de Production
Les contrôles en cours de production (In-Process Controls) permettent de détecter immédiatement toute dérive du processus :
Contrôles dimensionnels : Vérification de dimensions critiques sur échantillons réguliers (toutes les heures, toutes les 100 pièces selon le plan de contrôle).
Contrôles visuels : Inspection à 100% ou par échantillonnage selon le niveau de criticité. Détection de défauts d'aspect (bavures, traces de brûlure, contamination).
Contrôles fonctionnels : Tests d'étanchéité, de résistance mécanique, d'assemblage sur des échantillons représentatifs.
Surveillance des paramètres machine : Enregistrement continu de la température, pression, vitesse d'injection, temps de cycle. Les systèmes modernes en 2026 intègrent des algorithmes d'intelligence artificielle détectant les dérives avant l'apparition de non-conformités.
Tests Finaux et Libération
Avant la libération d'un lot, une batterie de tests finaux est réalisée :
| Test | Méthode | Critère d'acceptation |
|---|---|---|
| Dimensions critiques | MMT (Machine à Mesurer Tridimensionnelle) | Selon plan de contrôle |
| Aspect visuel | Inspection 100% ou AQL | Absence de défauts critiques |
| Biocompatibilité | Selon ISO 10993 | Conformité aux tests applicables |
| Stérilité (si applicable) | Test de stérilité USP | Absence de croissance microbienne |
| Résistance mécanique | Traction, flexion, impact | Selon spécifications produit |
| Extractibles | Chromatographie GC-MS | Conformité aux limites définies |
| La libération du lot n'intervient qu'après revue complète de toute la documentation par une personne qualifiée (Qualified Person en Europe). | ||
Tendances et Innovations 2026
L'année 2026 est marquée par une accélération de l'innovation dans l'injection plastique médicale, portée par la digitalisation, les nouveaux matériaux et l'automatisation.
Automatisation et Industrie 4.0
L'Industrie 4.0 transforme radicalement les usines de production de dispositifs médicaux. Les technologies déployées en 2026 incluent :
Jumeaux numériques : Répliques virtuelles des machines et des processus, permettant de simuler et d'optimiser la production avant toute modification physique. Les jumeaux numériques sont utilisés pour prédire l'usure des moules, optimiser les paramètres d'injection, et former les opérateurs.
Maintenance prédictive : Capteurs IoT (Internet of Things) surveillant en temps réel l'état des machines. Des algorithmes d'intelligence artificielle analysent les données pour prédire les pannes avant qu'elles ne surviennent, réduisant les temps d'arrêt non planifiés de 35% en moyenne.
Traçabilité blockchain : Certains fabricants pionniers implémentent la blockchain pour assurer une traçabilité inaltérable de bout en bout, de la matière première au patient final.
Vision artificielle avancée : Systèmes de contrôle qualité basés sur l'intelligence artificielle, capables de détecter des défauts invisibles à l'œil humain avec une fiabilité supérieure à 99,9%.
Matériaux Biosourcés
La pression environnementale pousse l'industrie vers des polymères plus durables. En 2026, plusieurs matériaux biosourcés obtiennent les certifications nécessaires pour les applications médicales :
PLA médical : Polylactide issu de ressources renouvelables, biocompatible et biodégradable. Utilisé pour les dispositifs temporaires (fils de suture résorbables, implants biodégradables).
Bio-PE et Bio-PP : Polyéthylène et polypropylène d'origine végétale, chimiquement identiques à leurs équivalents fossiles mais avec une empreinte carbone réduite de 70%.
Polymères à base d'algues : Recherches prometteuses sur des biopolymères issus d'algues, offrant des propriétés mécaniques comparables aux polymères conventionnels.
📊 Croissance annuelle de 18% entre 2024 et 2026, atteignant 2,3 milliards d'euros - Marché des biopolymères médicaux
Intelligence Artificielle pour le Contrôle Qualité
L'IA révolutionne le contrôle qualité en 2026 :
Détection de défauts en temps réel : Caméras haute résolution couplées à des réseaux de neurones convolutifs inspectent chaque pièce à la sortie du moule. Le taux de détection atteint 99,95%, contre 95% pour l'inspection humaine.
Optimisation automatique des paramètres : Les systèmes d'IA ajustent automatiquement les paramètres d'injection pour maintenir la qualité optimale, même en cas de variations de la matière première ou de conditions ambiantes.
Prédiction de la qualité : Analyse des données historiques pour prédire la probabilité de non-conformité avant même le début de la production.
Impression 3D Hybride
La convergence entre injection plastique et impression 3D donne naissance à des processus hybrides :
Moules imprimés en 3D : Fabrication rapide de moules prototypes en résines haute performance, réduisant les délais de développement de 60%.
Inserts imprimés : Intégration d'inserts complexes fabriqués par impression 3D métal dans des pièces injectées, combinant la précision de l'injection avec la liberté de conception de l'additif.
Production de petites séries : Pour les dispositifs personnalisés ou les marchés de niche, l'impression 3D complète l'injection plastique, offrant une flexibilité inégalée.
Questions Fréquentes (FAQ)
Quelle est la différence entre un plastique médical et un plastique industriel standard ?
Un plastique médical doit répondre à des exigences de biocompatibilité strictes définies par la norme ISO 10993. Il est testé pour s'assurer qu'il ne provoque aucune réaction toxique, allergique ou inflammatoire au contact du corps humain. Les plastiques médicaux sont produits dans des conditions contrôlées, avec une traçabilité complète de chaque lot. Ils sont exempts d'additifs potentiellement dangereux (phtalates, bisphénol A dans certaines applications) et peuvent être stérilisés sans dégradation de leurs propriétés. Le coût d'un polymère médical est généralement 2 à 5 fois supérieur à celui d'un polymère industriel standard.
Combien coûte la certification ISO 13485 pour un fabricant de pièces plastiques médicales ?
Le coût de la certification ISO 13485 varie considérablement selon la taille de l'entreprise, la complexité des processus et le niveau de maturité du système qualité existant. Pour une PME, l'investissement initial (mise en conformité + certification) se situe entre 50 000 € et 150 000 €. Cet investissement inclut la formation du personnel, la mise en place de procédures, l'audit de certification initial, et les éventuels audits complémentaires. Les coûts récurrents (audits de surveillance annuels, maintenance du système qualité) représentent ensuite 15 000 € à 30 000 € par an. Le retour sur investissement est généralement atteint en 2 à 3 ans grâce à l'accès à de nouveaux marchés et à l'amélioration de l'efficacité opérationnelle.
Quels sont les délais typiques pour développer et valider un nouveau dispositif médical en injection plastique ?
Le développement complet d'un dispositif médical injecté, de la conception initiale à la commercialisation, nécessite généralement 18 à 36 mois. Ce délai se décompose ainsi : conception et prototypage (3-6 mois), développement et qualification du moule (4-8 mois), validation du processus de fabrication (3-6 mois), tests de biocompatibilité et autres tests réglementaires (6-12 mois), préparation du dossier réglementaire et obtention des autorisations (6-12 mois). Les dispositifs de classe III (haut risque) nécessitent des délais plus longs en raison d'exigences cliniques supplémentaires. La planification rigoureuse et l'implication précoce des experts réglementaires sont essentielles pour respecter ces délais.
Comment choisir un fabricant qualifié pour l'injection de pièces plastiques médicales ?
Le choix d'un fabricant de pièces plastiques médicales doit s'appuyer sur plusieurs critères essentiels : certification ISO 13485 en cours de validité (vérifier les certificats auprès de l'organisme certificateur), expérience démontrée dans le secteur médical avec références vérifiables, capacité de production en salle blanche avec classification appropriée (ISO 7 ou 8), maîtrise des techniques d'injection spécifiques à votre application (micro-injection, bi-injection, etc.), système de gestion des risques robuste selon ISO 14971, capacité de validation complète des processus, et services de support technique et réglementaire. Un audit sur site est fortement recommandé avant toute décision d'engagement. Privilégiez les fabricants transparents sur leurs processus et disposés à établir un partenariat à long terme.
Quelles sont les erreurs courantes à éviter dans le développement d'un dispositif médical injecté ?
Les erreurs les plus fréquentes incluent : sous-estimer les exigences réglementaires et les intégrer trop tardivement dans le projet (coûteux en modifications), choisir un matériau sans considération suffisante de la biocompatibilité et de la processabilité, négliger la conception pour la fabrication (DFM - Design for Manufacturing), ce qui conduit à des moules complexes et coûteux, ne pas prévoir suffisamment de temps et de budget pour la validation du processus, omettre de définir clairement les caractéristiques critiques pour la qualité (CTQ) dès la conception, ne pas impliquer le fabricant d'injection suffisamment tôt dans le développement, et sous-estimer les coûts de qualification et de validation (généralement 20 à 30% du budget total de développement). Une approche collaborative entre le concepteur, le fabricant et les experts réglementaires dès les phases initiales permet d'éviter ces écueils.
Chiffres Clés
📊 78% des fabricants de dispositifs médicaux ont augmenté leurs investissements dans l'injection plastique de précision en 2026 (Source: Gartner Medical Device Survey 2026)
💡 34% d'augmentation de l'utilisation de polymères biosourcés dans les dispositifs médicaux entre 2024 et 2026 (Source: Medical Plastics News 2026)
🏭 35% de réduction des temps d'arrêt non planifiés grâce à la maintenance prédictive basée sur l'IA (Source: Industry 4.0 Medical Manufacturing Report 2026)
🌍 2,3 milliards € : Valeur du marché européen des biopolymères médicaux en 2026, avec une croissance annuelle de 18% (Source: European Bioplastics Association 2026)
Conclusion
L'injection de pièces plastiques pour dispositifs médicaux en 2026 représente un secteur à la croisée de l'excellence technique, de la rigueur réglementaire et de l'innovation technologique. Les fabricants qui réussissent sont ceux qui maîtrisent simultanément les fondamentaux du moulage par injection, les exigences normatives strictes (ISO 13485, FDA 21 CFR Part 820, marquage CE), et les technologies émergentes comme l'Industrie 4.0 et l'intelligence artificielle.
Les tendances de 2026 - automatisation avancée, matériaux biosourcés, contrôle qualité intelligent - ne sont pas de simples évolutions incrémentales, mais des transformations profondes qui redéfinissent les standards de l'industrie. Les entreprises qui investissent aujourd'hui dans ces technologies se positionnent comme les leaders de demain.
Pour les responsables R&D, ingénieurs et acheteurs du secteur médical, le message est clair : le choix d'un partenaire de fabrication ne doit pas se limiter à des considérations de coût et de délai. La capacité à garantir la conformité réglementaire, la traçabilité complète, et l'innovation continue sont les véritables critères de sélection qui assureront le succès de vos dispositifs médicaux sur le long terme.
Vous développez un dispositif médical nécessitant des pièces injectées de haute précision ? Assurez-vous de sélectionner un fabricant certifié ISO 13485, disposant d'une expertise démontrée dans votre domaine d'application, et capable de vous accompagner de la conception à la commercialisation. L'avenir de votre projet en dépend.